Atteintes neurocognitives (DSM V)
Délirium, maladie d’Alzheimer, démence vasculaire, maladie à corps de Lewy et démence fronto-temporale

Dans le DSM V (APA, 2013), les atteintes neurocognitives (neurocognitive disorders) sont décrites comme un groupe d’atteintes acquises dans lesquelles un déficit clinique primaire est observé dans une ou plusieurs fonctions cognitives (traduction libre). L’atteinte cognitive observée n’est donc ni présente à la naissance ni dans les premières années de vie. Le déclin cognitif noté est l’atteinte principale que vit la personne, quand son fonctionnement cognitif est comparé à son niveau de fonctionnement antérieur. Cette atteinte, quand elle est majeure, était nommée démence dans les DSM antérieurs. L’atteinte plus légère était présentée comme l’atteinte cognitive légère (mild cognitive impairmentf). Bien que les écrits du DSM V proposent une nouvelle nomenclature pour les démences, les atteintes cognitives n’en restent pas moins des regroupements de symptômes dont l’expression les distingue l’une de l’autre. La précision diagnostique nous ramène aux pathologies que nous connaissons depuis longtemps. Nous verrons ici le délirium, qui n’est pas en soi une démence et les quatre atteintes neurocognitives les plus fréquemment rencontrées dans la population Canadienne, soit celles causées par : la maladie d’Alzheimer, l’atteinte fronto-temporale, la maladie à corps de Lewy et la démence vasculaire.
Description / Définition
Dans sa définition la plus globale, l’atteinte neurocognitive consiste en une détérioration cognitive globale, progressive et irréversible altérant les capacités à réaliser les activités quotidiennes de façon autonome, les plus complexes et les plus simples. L’atteinte de la mémoire et des capacités d’apprentissage est le symptôme le plus fréquent et le plus prédominant des atteintes neurocognitives, mais les types d’atteintes, leur sévérité, leur durée, la nature des problèmes de comportements qui les accompagnent font en sorte que chacune des personnes présentera un tableau clinique qui lui sera propre. L’étiologie des atteintes étant le plus souvent inconnue, sauf pour le faible pourcentage des personnes ayant une atteinte nettement génétique, les traitements offerts sont palliatifs et de soutien, pour la personne et ses proches.
Il est important de noter que le délirium, qui mime l’atteinte neurocognitive légère ou sévère, peut avoir pour origine une ou des problématiques cardiovasculaires, endocrines, tumorales, métaboliques, infectieuses ou toxicologiques qui peuvent être corrigées. Le traitement de la cause physiologique du délirium fait en sorte que les personnes retrouvent leur fonctionnement cognitif antérieur, donc la situation est réversible, ce qui n’est pas vu dans les atteintes neurocognitives de type démence. Le délirium est donc une classe à part d’atteinte neurocognitive. La dépression chez la personne âgée peut aussi mimer l’atteinte neurocognitive. Elle a été longtemps qualifiée de pseudo-démence dans le cadre de l’établissement du diagnostic différentiel.
Les domaines cognitifs qui peuvent être touchés dans le déclin observé chez les personnes qui vivent une atteinte neurocognitive sont :
- L’attention complexe
- Les fonctions exécutives
- Les capacités d’apprentissage et la mémoire
- Le langage
- Les fonctions perceptivo-motrices
- La cognition sociale

Le tableau clinique observé chez chacune des personnes atteintes sera unique, les fonctions atteintes variant selon les diverses origines possibles des atteintes cognitives et divers facteurs provoquant des degrés d’atteintes variables pour chacune des fonctions neurocognitives, modulant le déclin cognitif et la réaction des personnes à ce dernier, pour l’autonomie et pour l’affect.
Les atteintes neurocognitives les plus fréquemment vues chez les personnes suivies en réadaptation au Canada ont pour origine: la maladie d’Alzheimer, la démence vasculaire, la démence à corps de Lewy et l’atteinte fronto-temporale. En voici une brève description, qui sera suivie plus loin des critères diagnostics selon le DSM V.
Maladie d’Alzheimer
La maladie d’Alzheimer est l’atteinte neurocognitive la plus fréquente chez la personne âgée, soit de 60 à 80 % de toutes les atteintes neurocognitives. Elle se caractérise par une atrophie du cortex cérébral des lobes frontaux, pariétaux et temporaux et de la région de l’hippocampe. Cette atrophie est causée par une accumulation de plaques de β-amyloïdes et d’enchevêtrements neurofibrillaires dans le cortex et la matière blanche sous-corticale. Elle entraîne une détérioration cognitive progressive, d’abord habituellement de la mémoire et des capacités d’apprentissage, puis dans toutes les sphères cognitives (voir https://www.youtube.com/watch?v=WwjaVWx-v_w en 3m 20sec.)
Démence vasculaire
La démence vasculaire résulte d’une série d’infarctus cérébraux focaux et diffus qui mènent à une détérioration cognitive en paliers aigus et à plus long terme à un déclin cognitif plus global et progressif. Elle a donc pour origine, dans la plupart des cas, une maladie vasculaire cérébrale. Il s’agit de la deuxième cause la plus commune d’atteinte neurocognitive chez la personne âgée. Les symptômes de cette atteinte sont représentatifs des lésions focales, mais un déclin continu dans toutes les fonctions cognitives est éventuellement observé.
Maladie à corps de Lewy
La maladie à corps de Lewy se caractérise par l’apparition, dans le cytoplasme des neurones du cortex cérébral, d’inclusions cellulaires appelées «corps de Lewy», qui entraînent une dégénérescence cognitive. Il s’agit du troisième type le plus commun d’atteinte neurocognitive. Les symptômes sont d’abord cognitifs, toutes les fonctions pouvant être atteintes, puis, au moins un an plus tard au moins, la personne présentera des signes de parkinsonisme. Il est important de noter que l’atteinte cognitive précède l’apparition des signes de parkinsonisme, contrairement à la démence qui accompagne la maladie de Parkinson, alors que les signes de parkinsonisme apparaissent les premiers. La fluctuation rapide des symptômes est, entre autres, ce qui permet de différencier cette atteinte neurocognitive des autres types d’atteintes.
Atteinte fronto-temporale ou frontale
L’atteinte fronto-temporale ou frontale est relative à des troubles sporadiques affectant les lobes frontaux et temporaux du cerveau, provoquant d’abord des changements notables de la personnalité et/ou du langage, suivis d’atteintes de toutes les autres fonctions cognitives. La maladie de Pick, qui consiste en un agrandissement des sillons du cortex des régions frontale et temporale, en est la forme la plus fréquente. Elle se distingue des autres formes principalement par les changements remarquables dans la personnalité, précédent le plus souvent les troubles mnésiques. Environ 10% des cas d’atteintes neurocognitives sont attribuables à cette atteinte fronto-temporale.
La maladie d’Alzheimer est bien décrite dans le reportage qui peut être retrouvé au : http://www.lemonde.fr/sciences/video/2013/09/20/la-maladie-d-alzheimer-expliquee-3-minutes_3481421_1650684.html (3m 8sec.)
L’atteinte fronto-temporale est présentée sous forme de témoignage au : http://www.youtube.com/watch?v=bNtNm2uNUH0 (6m 16sec.)
Le délirium
Le délirium est une atteinte neurocognitive secondaire à un problème physiologique. Les critères diagnostics en sont, selon la classification du DSM V :
- Perturbation de l’attention et de la conscience;
- Qui se développe rapidement (quelques heures/jours), constituant un changement dans le niveau de fonctionnement habituel de la personne, et fluctuant en intensité au cours d’une même journée;
- Où l’on observe au moins une autre perturbation dans un domaine cognitif;
- Ne s’expliquant pas autrement, par un autre trouble du SNC, et ne résultant pas d’une atteinte importante de l’état d’éveil, comme dans un coma;
- Les examens révélant l’existence d’une atteinte physiologique, d’une intoxication ou d’un sevrage expliquent directement le tableau clinique du délirium vécu par la personne.
Quand la personne, un proche ou un intervenant soupçonne que la personne développe une atteinte neurocognitive, il faudra préciser, dans la démarche diagnostique, divers éléments qui seront essentiels pour établir un plan d’intervention. Il faudra donc déterminer d’abord s’il y a réellement présence d’une atteinte neurocognitive et si cette dernière semble légère ou majeure.
La résolution de l’atteinte physiologique entraîne le plus souvent la restauration du statut cognitif habituel de la personne. L’observation d’une autre atteinte cognitive (critère C), peut relever d’une atteinte de la mémoire, d’une désorientation, d’un problème de langage ou d’un problème perceptuel. Le cycle veille/sommeil est souvent perturbé pendant la période de délirium (somnolence diurne, agitation ou éveil nocturne, difficultés d’endormissement, inversement complet du cycle). Le délirium peut aussi provoquer des perturbations émotionnelles (anxiété, peurs, dépression, irritabilité, colère, euphorie, apathie, etc.) ainsi que des changements subits et imprévisibles entre différents états émotifs. Des hallucinations seront parfois observées, étant le plus souvent visuelles. Ces signes seront le plus souvent observés la nuit ou dans des conditions où les stimulations et les indices environnementaux sont faibles. Le facteur diagnostic déterminant sera l’atteinte de l’attention ou du niveau de conscience, en comparaison au niveau habituel de la personne. Le diagnostic de délirium sera finalement complété de la mention de l’agent causal, de la durée de ce dernier et de l’état d’agitation de la personne :
- Aigu : quelques heures/jours
- Chronique : quelques semaines/mois
- Hyperactif : est plus facilement repéré par les soignants et le plus souvent induit par une intoxication ou un sevrage (substances toxiques, mais aussi médication)
- Hypoactif : survient plus souvent chez les personnes plus âgées.
Étiologie du délirium
La cause la plus fréquente de délirium est d’origine physiologique initialement. Il peut donc être :
- Dû à l’intoxication avec une substance;
- Dû au sevrage d’une substance;
- Induit par une médication;
- Dû à une condition médicale autre : infection, dérèglement métabolique, etc.;
- Dû à de multiples étiologies.
Données populationnelles pour le délirium
Dans la population canadienne, en 2010, les personnes suivantes avaient vécu un délirium :
- 1 à 2% de la population générale et 14% chez les plus de 85 ans;
- Environ 60% des personnes hébergées en centres de soins de longue durée;
- En fin de vie, environ 80% des personnes.
Facteurs de risque : toxicomanie, alcoolisme, polypharmacie, atteintes du SNC, toute atteinte physiologique, inactivité, immobilité, chutes, mais surtout l’âge avancé en combinaison avec un des facteurs qui précèdent. Les personnes ayant une atteinte mineure ou majeure de la neurocognition seront plus à risque, à savoir que le délirium survient souvent chez les personnes qui ont une atteinte cognitive sous-jacente.
Pronostic pour le délirium
L’agent causal du délirium sera déterminant du pronostic, autant pour le retour au niveau de fonctionnement cognitif antérieur, que pour le déclin fonctionnel, les séquelles cognitives ou le décès. Plus l’intervention sur l’état causal sera rapide, si possible, plus court sera le délirium. Le délirium associé à une atteinte qui provoque un déclin de l’autonomie risque d’engendrer une hospitalisation, qui à son tour aggravera le délirium et pourra provoquer un déclin plus rapide des fonctions cognitives.
Atteintes neurocognitives légères et sévères
La nomenclature décrite dans le DSM V propose d’abord de différencier les atteintes sévères (majeures) des atteintes légères (mineures). Les critères diagnostics proposés pour cette première différenciation des atteintes neurocognitives est la suivante :
| ATTEINTE NEURO-COGNITIVE MAJEURE (sévère) |
CRITÈRES DIAGNOSTICS :
|
|
ATTEINTE NEURO-COGNITIVE |
CRITÈRES DIAGNOSTICS :
|
Dans les versions antérieures des DSM, l’atteinte majeure (sévère) était nommée démence alors que l’atteinte mineure (légère) était nommée atteinte cognitive légère (mild cognitive impairment) et faisait l’objet d’un diagnostic en soi. Cette distinction réalisée, l’atteinte neurocognitive sera associée, dans la démarche diagnostique, à son principal facteur causal parmi un ensemble de causes probables ou possibles : maladie d’Alzheimer, atteinte fronto-temporale, atteinte vasculaire, la maladie à corps de Lewy, le traumatisme crânio-cérébral, la maladie des prions, l’abus de substances, l’infection au VIH, la maladie de Parkinson, la maladie de Huntington et les autres. Les causes des atteintes neurocognitives sont nombreuses, mais les quatre premières de cette liste sont les plus fréquentes dans la population. Nous les verrons plus en détail plus loin dans ce document.
Données populationnelles relatives aux atteintes neurocognitives
Incidence et prévalence au Canada
La prévalence de l’atteinte neurocognitive est deux fois plus élevée chez les femmes que chez les hommes. En 2010, au Canada, il était estimé que 500 000 Canadiens étaient atteints de la maladie d’Alzheimer ou d’une affection connexe (soit une atteinte neurocognitive majeure). Au même moment, il est estimé que 35 millions de personnes dans le monde sont atteintes de la maladie d’Alzheimer ou d’une affection connexe. Il est prévu que dans les prochaines années, l’incidence (nombre de nouveaux cas annuellement) des atteintes neurocognitives chez les personnes âgées explosera. La Société Alzheimer prévoit 115 000 millions cas mondialement en 2050. L’atteinte neurocognitive majeure est actuellement la cause la plus importante des pertes fonctionnelles chez les 65 ans et plus au Canada.
Facteurs de risques et de protection
Au-delà des causes identifiées au « diagnostics », comme la maladie d’Alzheimer, les causes exactes des premières atteintes les plus fréquentes (Alzheimer, vasculaire, à corps de Lewy et fronto-temporale) ne sont pas très bien connues. Plusieurs facteurs de risque semblent cependant se démarquer, même s’ils ne sont pas tous démontrés hors de tout doute dans la recherche sur le sujet :
- Âge : le grand âge est le facteur de risque le plus important;
- Pour la maladie d’Alzheimer, la présence de l’allèle apoE4 de l’apolipoprotéine E (>75 ans, le risque est de 10 à 30 fois plus élevé chez les porteurs de cet allèle);
- Faible niveau d’éducation;
- Historique de traumas crâniens avec perte de conscience;
- Historique de dépression;
- Âge (avancé) de la première grossesse;
- Exposition environnementale et professionnelle (ex : aluminium);
- Exposition à des toxines présentes dans l’environnement;
- Historique de thérapie électroconvulsive;
- Abus d’alcool ou de substances analgésiques;
- Inactivité physique de longue durée (déconditionnement);
- Facteurs de risques vasculaires (ex : hypertension, hypercholestérolémie);
- Diabète de type 2;
Cependant, divers facteurs de protection ou de prévention sont aussi identifiés, principalement pour la maladie d’Alzheimer, même s’ils ne sont pas tous démontrés hors de tout doute dans la recherche sur le sujet :
- Présence de l’allèle apoE2 de l’apolipoprotéine E;
- Modération de la consommation d’alcool;
- Adoption une diète riche en acides gras oméga-3 et pauvre en gras saturés (ex : poisson);
- Exposition à des antioxydants (ex : vitamine E);
- Contrôle de l’hypertension;
- Pratique régulière d’activités physiques;
- Contrôle des niveaux de cholestérol;
- Exécution d’activités qui représentent un défi mental (ex : apprendre de nouvelles choses, faire des mots croisés, utiliser certains logiciels de mise en forme cognitive, etc.);
- Oestrogénothérapie substitutive postménopausique;
- Usage d’anti-inflammatoires non stéroïdiens;
- Usage d’antihypertenseurs spécifiques;
- Usage de statines;
- Usage d’antihistaminiques spécifiques.
Étiologie des atteintes neurocognitives
L’étiologie de la maladie d’Alzheimer et d’un bon nombre d’atteintes neurocognitives reste encore inconnue. Cependant, il existe une plus grande probabilité de développer la maladie chez les gens âgés de plus de 65 ans, ce qui fait de l’âge le plus grand facteur de prédiction de ces atteintes.
Les recherches actuelles les plus nombreuses s’intéressent au domaine de la génétique et montrent que dans environ 5 à 15% des cas d’atteintes neurocognitives, il est possible d’observer une tendance familiale. Pour ces atteintes d’origine génétique, le développement de la maladie sera souvent plus précoce, soit avant 65 ans. Par exemple, dans la maladie d’Alzheimer d’origine génétique, il a été démontré qu’une mutation du gène responsable de la protéine précurseur de l’amyloïde (PPA) semble mener à une forme autosomale dominante de la maladie, déclenchée de façon précoce. L’altération de cette protéine provoque une agrégation fibrillaire et une accumulation de β-amyloïdes qui entraînent la mort des neurones et la formation d’enchevêtrements neurofibrillaires et de plaques séniles, qui consistent en une accumulation d’axones et de dendrites dégénérées, d’astrocytes et de cellules gliales autour d’un noyau amyloïde. Cette cause génétique serait responsable d’environ 10% des cas de maladie d’Alzheimer. Un pourcentage similaire d’atteintes génétiques est démontré chez les personnes qui développent la maladie dans la moyenne d’âge attendue ou tardivement alors que le polymorphisme au niveau des allèles de l’apolipoprotéine E (apoE ou ε) pourrait avoir une influence quant à l’accumulation de β-amyloïdes, l’intégrité du cytosquelette et l’efficacité de la régénérescence neuronale. La présence de l’allèle apoE4, par exemple, aggraverait le risque de développer la maladie d’Alzheimer, tandis que celle de l’allèle apoE2 réduirait ce risque.
Dans la majorité des autres types d’atteintes neurocognitives plus fréquentes, soit la démence vasculaire, la maladie à corps de Lewy et l’atteinte fronto-temporale, et même pour la maladie d’Alzheimer qui ne semble pas d’origine génétique, que les atteintes soient majeures ou mineures, si les processus anatomo-physiologiques conduisant à la maladie sont connus, les causes de leur instauration chez les personnes atteintes restent encore à être élucidées.
Pathogenèses des atteintes neurocognitives
Les résultats d’examens macroscopiques et microscopiques des cellules cérébrales ont permis de déterminer la pathogenèse de la plupart des atteintes neurocognitives les plus fréquentes.
La pathophysiologie de la maladie d’Alzheimer consiste en l’accumulation de dépôts de β-amyloïdes et d’enchevêtrements neurofibrillaires intracellulaires qui peuvent s’avérer toxiques pour le système nerveux et nuire à la conduction de l’influx nerveux. Les plaques neurofibrillaires se développent d’abord dans l’hippocampe, ce qui provoque des problèmes de mémoire et d’apprentissage, et c’est l’inverse pour les plaques amyloïdes qui se développent ailleurs dans le cerveau. L’hypothèse actuelle est que les plaques séniles seraient les précurseurs de la formation des plaques neurofibrillaires. Le nombre de plaques séniles ainsi que leur localisation dans le cerveau sont les facteurs déterminants de l’altération des fonctions cognitives qui sera observée chez les personnes atteintes.
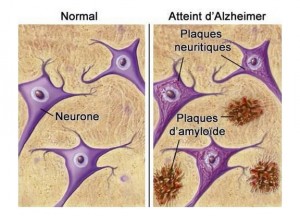
On observe aussi chez les personnes atteintes de la maladie d’Alzheimer une diminution de l’utilisation du glucose cérébral et de la perfusion dans le lobe pariétal et les cortex temporal et préfrontal. Il est aussi possible d’observer une augmentation de la concentration de protéines tau, composantes des enchevêtrements neurofibrillaires et des β-amyloïdes, dans le cerveau et le liquide céphalorachidien de ces personnes. La concentration de choline acéthyltransférase est plutôt diminuée chez les personnes atteintes, menant à un déficit en acétylcholine. Les niveaux de divers autres neurotransmetteurs dont la norépinephrine, l’acide gamma-aminobutyrique (GABA) et le glutamate se voient aussi modifiés.
Bien que la pathogenèse de la maladie d’Alzheimer soit complexe, elle explique les symptômes observés chez la personne atteinte dans la mesure où le fonctionnement cognitif est perturbé par le dépôt des plaques et les anomalies fonctionnelles de la transmission synaptique. Une présentation de la pathogenèse est proposée ici: http://www.youtube.com/watch?v=HyP82JP-z9w (6m 26sec.).
Pour l’atteinte neurocognitive d’origine vasculaire, qui est la deuxième plus fréquente après la maladie d’Alzheimer, le processus pathologique est lié à une « maladie » du système vasculaire cérébral. On y retrouve une atteinte des petits vaisseaux cérébraux, fréquente chez la personne âgée, qui provoque de petits infarctus entraînant des micro-lacunes dans la substance blanche péri-ventriculaire cérébrale qui sera responsable des déficits cognitifs qui seront observés. La localisation des infarctus sera déterminante des symptômes qui seront alors dits focaux. Chaque infarctus cérébral qui se produira provoquera l’apparition de nouveaux symptômes dans le déclin cognitif associé à cette atteinte.
Dans la maladie à corps de Lewy, ce sont les corps de Lewy qui seront tenus responsables de l’apparition des problèmes cognitifs chez la personne atteinte. Dans le processus pathologique de cette atteinte, il sera observé des dépôts anormaux de protéine alpha-synucléine à l’intérieur des cellules cérébrales. Ces dépôts formeront les corps de Lewy, du nom du chercheur les ayant le premier décrits, qui pourront interrompre la transmission nerveuse. Le processus qui provoque la formation des corps de Lewy est encore inconnu à ce jour. Cette atteinte neurocognitive peut se développer simultanément à la maladie d’Alzheimer ou à la maladie de Parkinson, en ses stades plus tardifs. Elle est moins fréquente que les deux précédentes, mais compte tout de même pour environ 10% des atteintes neurocognitives.
La démence fronto-temporale, dont une forme est la maladie de Pick, est plus rare, mais très distincte des autres formes d’atteintes neurocognitives. La cause de cette atteinte est encore inconnue, mais elle résulte de la destruction neuronale dans les régions cérébrales frontales, temporales et parfois pariétales. Une origine génétique, familiale, est reconnue dans 30% des cas, impliquant le gène tau et/ou celui de la progranuline. Les lésions retrouvées dans la démence fronto-temporale semblent la résultante d’inclusions protéiques toxiques ou mutées dans les cellules neuronales. Certaines formes sont aussi d’origine histologique non spécifiée, à savoir que la destruction neuronale est observée, les lobes atrophiés, sans cause précise identifiable, même à l’autopsie. Cette atteinte neurocognitive, toute forme de démence fronto-temporale, provoque des signes singuliers de changements dans la personnalité ou de perturbation du langage, ces deux formes coexistant le plus souvent.
Les autres formes d’atteintes neurocognitives, comme celles secondaires à la maladie de Parkinson, de Huntington, au VIH, aux traumatismes cranio-cérébraux, etc., ont pour origine le processus pathologique qui sous-tend la maladie primaire.
Signes et symptômes des atteintes neurocognitives
Toutes les formes d’atteintes neurocognitives partagent un tableau clinique de base qui permet d’identifier initialement que les personnes vivent ce type d’atteinte. L’installation insidieuse des premiers symptômes et le déclin cognitif qui pourra être observé constituent la base commune de ces atteintes. Les premiers signes et symptômes communs seront le plus souvent :
- Détérioration de la mémoire à court terme, ce qui rend l’apprentissage et la rétention de nouvelles informations difficile et éventuellement impossible alors que la mémoire des événements plus lointains sera atteinte;
- Difficultés de langage, notamment pour trouver le mot juste (difficulté d’accès lexical ou manque du mot);
- Variations de l’humeur;
- Changements dans la personnalité qui seront plus légers initialement et de plus en plus importants dans l’évolution de l’atteinte;
- Difficulté graduelle à effectuer des activités quotidiennes complexes (ex: gestion financière, orientation géographique, etc.) puis plus simples (se nourrir, se vêtir, etc.). L’aide requise pour ces activités sera de plus en plus grande;
- Détérioration des capacités de pensée abstraite, d’introspection et du jugement;
- Apparition de troubles comportementaux tels que l’irritabilité, l’hostilité, l’anxiété, le manque de coopération, la passivité, la dépression, l’agitation, l’errance, qui seront de plus en plus présents dans le cours de la maladie, éventuellement associés à l’altération des sensations et des perceptions, et la présence d’hallucinations et de délires.
Dans les stades très sévères de l’atteinte cognitive, la personne pourra avoir de la difficulté à se déplacer et se positionner, ne plus pouvoir réaliser ses activités quotidiennes, être incontinente, ne plus pouvoir communiquer, être totalement dépendante de ses proches aidants. Plusieurs échelles indicatrices du déclin associé aux atteintes neurocognitives sont proposées, celle de Reisberg étant probablement la plus connue :
L’échelle de détérioration globale, également appelée Échelle de Reisberg, permet aux professionnels de la santé de mesurer la progression de la maladie d’Alzheimer. L’échelle divise la maladie d’Alzheimer en sept stades de détérioration des capacités.
Stade 1 : Pas de déficit cognitif : N’éprouve aucune difficulté dans la vie quotidienne.
Stade 2 : Déficit cognitif très léger : Oublie les noms et l’emplacement des objets et peut avoir de la difficulté à trouver ses mots.
Stade 3 : Déficit cognitif léger : A de la difficulté à s’orienter dans un endroit inconnu et a de la difficulté à fonctionner au travail ou dans un contexte familier.
Stade 4 : Déficit cognitif modéré : A de la difficulté à accomplir des tâches complexes (finances, magasinage, planification d’un repas avec des invités).
Stade 5 : Déficit cognitif relativement grave : A besoin d’aide pour choisir ses vêtements et a besoin qu’on lui rappelle que c’est l’heure de la douche ou du bain.
Stade 6 : Déficit cognitif grave : Perd la notion des expériences et événements récents de sa vie, a besoin d’aide pour prendre son bain, ou a peur de prendre son bain, et a de plus en plus besoin d’aide pour aller aux toilettes ou est incontinent.
Stade 7 : Déficit cognitif très grave : Utilise un vocabulaire très restreint qui se réduira bientôt à quelques mots seulement, perd la capacité de marcher et de s’asseoir, a besoin d’aide pour manger.
Bien que de telles classifications existent, il est important de noter que les symptômes se manifestent à divers moments dans la progression de la maladie en fonction du type d’atteinte et de façon unique pour chacune des personnes, la présence et le moment d’apparition des symptômes variant significativement d’une personne à l’autre. D’ailleurs, les critères diagnostics des différents types d’atteintes neurocognitives les distinguent le plus souvent dans l’expression des symptômes et dans la progression du déclin associé à chacune. Voici les critères diagnostics pour les quatre atteintes les plus fréquentes :
|
ATTEINTE |
Pour la forme sévère, le diagnostic de maladie d’Alzheimer probable est posé :
Autrement, le diagnostic de maladie d’Alzheimer possible est posé. Pour la forme légère, le diagnostic de maladie d’Alzheimer probable est posé sur la base de la présence de la mutation génétique et le diagnostic de maladie d’Alzheimer possible est posé si les trois critères suivants sont observés :
d. Les déficits observés ne sont pas mieux expliqués par une autre atteinte à la santé mentale ou à la santé physique. |
Le diagnostic de maladie d’Alzheimer sévère probable serait posé si la mutation génétique ou si les trois critères sont identifiés (déclin mémoire et un autre domaine, déclin progressif et graduel, pas d’autre étiologie) et celui de possible si la mutation génétique n’est pas documentée ou les trois critères ne sont pas tous présents. Un diagnostic d’atteinte par maladie d’Alzheimer légère probable serait posé si la mutation génétique est possible et si les trois critères sont présents alors que le diagnostic d’atteinte légère possible serait posé en absence d’une atteinte génétique potentielle ou en l’absence d’un ou plusieurs des trois critères, alors que l’atteinte cognitive est légère.
Un témoignage fort intéressant sur les personnes qui vivent cette atteinte et leurs proches est proposé au : https://www.youtube.com/watch?v=xy0n4NsjwlI (12m 36sec.) et au : http://www.allodocteurs.fr/actualite-sante-a-ans-claudine-est-atteinte-de-la-maladie-d-alzheimer_8274.html.
|
ATTEINTE |
CRITÈRES DIAGNOSTICS :
|
Le diagnostic d’une atteinte vasculaire probable est posé si (un des suivants) :
- Les critères cliniques sont validés par la neuro-imagerie;
- Chacune des atteintes neurocognitives est temporairement liée à un événement vasculaire cérébral ou si;
- La maladie vasculaire est diagnostiquée sur la base du tableau clinique et sur la génétique.
Le diagnostic d’une atteinte vasculaire possible est posé si la neuro-imagerie n’a pas été réalisée.
Les tableaux cliniques sont très variables selon les sites des lésions, leur étendue et le type d’atteinte vasculaire. Le déclin des fonctions cognitives se fera plus en fluctuations et en marches d’escalier, mais globalement, les déficits vont s’accumuler et le déclin sera progressif. Le traitement de l’information se fera typiquement plus lentement. Pour le diagnostic d’une atteinte légère, une seule atteinte vasculaire est notée, soit un ensemble de symptômes cognitifs reliés à l’atteinte d’un seul territoire cérébral alors que pour l’atteinte sévère, deux ou plusieurs atteintes vasculaires seront notées en lien avec les signes focaux présents.
|
ATTEINTE |
CRITÈRES DIAGNOSTICS :
|
L’atteinte neurocognitive fronto-temporale sera dite probable si il y a évidence de mutation génétique ou si l’atteinte des lobes frontaux ou temporaux (atrophie) est mise en évidence à l’IRM.
L’atteinte de la personnalité ou du langage, graduelle et progressive, avec des changements qui provoqueront l’adoption de comportements « inappropriés » seront d’abord observés, avant les problèmes mnésiques, et très clairement. Il faut noter que plusieurs personnes ayant une démence fronto-temporale auront une atteinte simultanée de la personnalité et du langage. Les changements observés peuvent être, par exemple, un changement dans les croyances religieuses, dans la vie sociale, dans les croyances politiques, un syndrome de Diogène (hoarding), des changements des comportements alimentaires. Le déclin cognitif est moins prédominant initialement, alors que seront observés des signes plus discrets de troubles de la planification et de l’organisation, de la distractibilité, un manque de jugement et/ou raisonnement abstrait, etc. Cette atteinte est plus fréquemment diagnostiquée chez les moins de 65 ans, comparativement aux autres atteintes neurocognitives, et compte pour environ 5% des cas d’atteintes neurocognitives.
| ATTEINTE NEURO-COGNITIVE à corps de Lewy |
CRITÈRES DIAGNOSTICS :
|
La démence à corps de Lewy est probablement l’atteinte neurocognitive la plus trompeuse en raison des fluctuations remarquables dans l’intensité des symptômes que vit la personne, sur de courtes périodes de temps. Dans une même journée, la personne peut sembler totalement « normale » puis totalement « absente ». En plus des éléments notés dans les critères diagnostics, il est possible que la personne vive de la dépression, des illusions et des hallucinations, le plus souvent auditives et non menaçantes, qu’elle souffre de somnambulisme (Rapid eye movement sleep behavior disorder = trouble du sommeil paradoxal), qui pourrait être à l’occasion un signe précurseur de cette atteinte. Les personnes souffrant de cette atteinte peuvent aussi avoir des chutes à répétition, des syncopes (pertes de conscience), de l’hypotension orthostatique et de l’incontinence urinaire.
Une atteinte légère sera diagnostiquée si les atteintes cognitives ne sont pas suffisamment significatives.
Moins fréquente que la maladie d’Alzheimer soit de 0.1 à 5% de la population âgée, elle semble un peu plus fréquente chez les hommes que chez les femmes.
Finalement, il est intéressant de noter que ces quatre atteintes neurocognitives ont en commun la présence d’une atteinte plus légère qui semble précurseur de la maladie plus sévère. Plusieurs chercheurs identifient « l’atteinte cognitive légère » (mild cognitive impairment) comme une atteinte en soi qui conduira éventuellement la grande majorité des personnes vers une des atteintes neurocognitives majeure. On observe, en signe initial, chez les personnes qui en sont atteintes, une dégradation de la mémoire sans atteinte significative de leur autonomie.
Dans ce déclin des fonctions cognitives, il est primordial de concevoir que certaines capacités sont encore présentes, que la personne vit encore une multitude d’émotions qu’elle comprend parfois difficilement. La dignité reste alors fondamentale et au cœur de la prise en charge.
Démarche diagnostique des atteintes neurocognitives
Il est primordial de distinguer les diverses atteintes neurocognitives des autres types d’affections semblables, dont le délirium, la dégradation naturelle de la mémoire survenant avec l’âge et les symptômes cognitifs liés à une dépression. Lorsque le diagnostic d’atteinte neurocognitive est cliniquement le plus probable, une démarche complexe s’amorce pour en distinguer le type précis. L’examen global de la personne inclura :
- L’histoire médicale, familiale et de l’atteinte vécue actuellement par la personne;
- Un examen bref de l’état mental ou cognitif de la personne (par exemple à l’aide du Mini-Mental State Examination);
- Un examen physique et neurologique complet;
- L’évaluation de l’état émotionnel (éliminer la dépression) et de l’environnement physique et social de la personne;
- Divers tests de laboratoire, le plus souvent pour éliminer les autres conditions possibles;
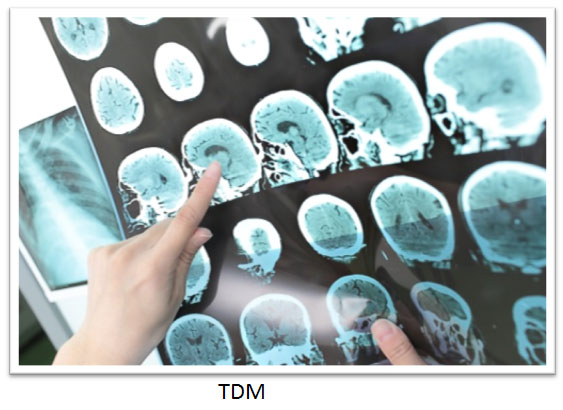
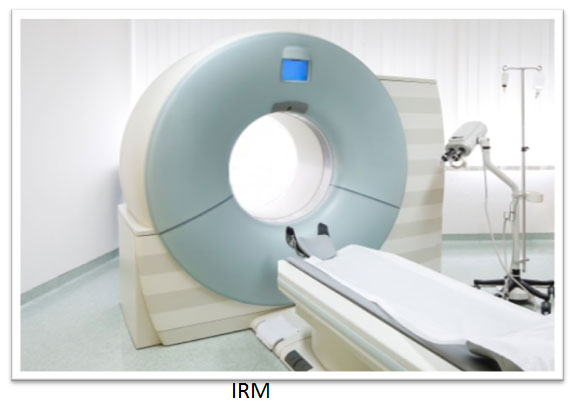
- L’examen en neuro-imagerie (TDM, pour son accessibilité, ou IRM, qui est plus précise, mais où les listes d’attente sont plus longues);
- Tests génétiques si le contexte s’y prête.
L’histoire de l’atteinte et les résultats cliniques sont le plus souvent assez fiables, ils permettraient de diagnostiquer environ 85% des personnes vivant une atteinte neurocognitive. Les critères diagnostics et les éléments spécifiques à chacun des types d’atteintes neurocognitives sont habituellement suffisants pour établir un diagnostic assez précis. Les causes fondamentales étant imprécises et les traitements possibles uniquement palliatifs, les imprécisions diagnostiques n’ont pas de conséquences dramatiques dans la vie des personnes. Il faut cependant noter que l’identification du type d’atteinte neurocognitive spécifique permet d’établir un plan d’intervention plus précis qui aide à anticiper un peu mieux le déclin à venir.
Conditions associées à l’atteinte neurocognitive
Hormis la dépression et le délirium, l’atteinte neurocognitive peut s’accompagner de divers états ou conditions qui ont un impact direct sur le cours de la maladie ou sur son expression. D’abord, les atteintes cognitives elles-mêmes, causées par l’a pathologie précise, auront un impact significatif sur le niveau d’autonomie des personnes, contribuant à la perte de la capacité fonctionnelle :
- Agnosie : incapacité à distinguer ou reconnaître des objets malgré des fonctions sensorielles intactes;
- Apraxie : incapacité à effectuer des gestes concrets ou symboliques indépendamment de tout autre trouble des fonctions motrices;
- Aphasie : perturbation du langage (expression et compréhension).
D’autre part, il est relativement fréquent de voir, chez une même personne, un amalgame de deux types d’atteintes neurocongitives, incluant une combinaison des maladie d’Alzheimer, de démence vasculaire, de démence à corps de Lewy et de démence fronto-temporale. De plus, toute atteinte cognitive antérieure à l’apparition d’une démence peut en être un facteur de risque significatif, comme les traumatismes cranio-cérébraux et la trisomie 21 (syndrome de Down).
Traitement médico-chirurgical et interprofessionnel
Il n’y a actuellement aucun traitement curatif qui peut être offert aux personnes souffrant d’atteintes neurocognitives. Certains traitements pharmacologiques sont prescrits aux personnes pour retarder le déclin cognitif vu dans l’atteinte, pour le contrôle des comportements perturbateurs ou pour la régulation de l’humeur. Ces traitements sont appréciables pour ralentir le déclin cognitif, non l’arrêter, chez les personnes qui « répondent » à cette pharmacopée et qui en tolèrent les effets secondaires, qui sont relativement importants surtout au début de la prise de ces médicaments :
Traitement pharmacologique
- Les inhibiteurs de la cholinestérase (ex : donepezil, rivastigmine, galantamine et tacrine) peuvent améliorer légèrement ou stabiliser les fonctions cognitives et la mémoire chez certaines personnes. Si aucun changement pouvant être dû à la médication n’est observé après quelques mois, le traitement est habituellement arrêté ou la médication changée. Ces médications sont recommandées pour les personnes qui souffrent d’une atteinte de légère à modérée. Les effets secondaires possibles affectent le système gastro-intestinal et peuvent aller jusqu’au vertige ou à l’arythmie cardiaque dans des cas extrêmes. Ces effets secondaires sont la principale raison de la cessation de la médication par les personnes ou leurs proches.
- La mémantine, un antagoniste des récepteurs de la N-methyl-D-aspartate, peut être administrée pour ralentir la progression de la maladie dans les phases plus sévères.
- Puisque la maladie s’accompagne, dans 25 à 30% des cas, d’une dépression, les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS) sont parfois prescrits aux personnes atteintes pour traiter les symptômes dépressifs qu’ils ressentent.
- Des essais cliniques ont été effectués avec un antihistaminique (Dimebon) qui améliorerait les fonctions neuronales et inhiberait la mort cellulaire, aidant à améliorer les fonctions cognitives des personnes atteintes. Les résultats ne sont, à ce jour, pas suffisamment probants pour généraliser une telle intervention.
- D’autres médications sont utilisées dans le traitement de symptômes spécifiques, comme les hallucinations et les comportements perturbateurs, variant selon les gens et les médecins.
Les recherches relatives au traitement des atteintes neurocognitives sont très actives et portent sur une variété d’options thérapeutiques, comme en témoignent certains reportages : http://ici.radio-canada.ca/emissions/telejournal/2013-2014/Reportage.asp?idDoc=326193 et http://zonevideo.telequebec.tv/media/2847/percee-dans-le-domaine-de-la-maladie-d-alzheimer/le-code-chastenay.
Interventions interprofessionnelles et ressources
Divers éléments constitutifs des atteintes neurocognitives demandent attention quand il est question d’offrir des interventions aux personnes et à leurs proches. L’atteinte étant multidimensionnelle, une approche interprofessionnelle est le plus souvent préconisée, généralement pour contenir certains symptômes et pour offrir du soutien aux proches de la personne atteinte. En voici quelques exemples :
- Pour traiter les symptômes comportementaux et psychologiques des atteintes neurocognitives, une approche écologique est recommandée avant que ne soit envisagé un traitement pharmacologique. Plusieurs stratégies sont proposées pour réduire l’impact des symptômes sur la personne et son entourage :
- Encourager la communication non verbale;
- Favoriser l’activité physique;
- Encourager la socialisation et les loisirs;
- Favoriser une routine;
- Adapter l’environnement pour favoriser l’utilisation des capacités résiduelles par la personne atteinte et atténuer les problèmes comportementaux.
- Il faut offrir du soutien aux proches aidants qui sont parfois les premiers à souffrir des troubles comportementaux des personnes atteintes. Le stress que peuvent vivre les aidants peut augmenter leurs risques de dépression, de troubles du sommeil et d’abus de substances. Il peut également mener à la négligence de la personne atteinte. Le soutien qui peut être offert est de diverses natures : journées d’activités extérieures pour la personne atteinte, temps de supervision au domicile par un aidant externe, prise en compte du fardeau de l’aidant pour l’accompagner dans sa recherche de ressources, etc.
- Il faut offrir du soutien et une intervention à la personne dans son environnement de vie habituel (sécurité, stimulation, activités qui ne sont pas sources de stress, astuces pour l’orientation, etc.) et adapter l’environnement aux capacités de la personne (ex : simplifier les stimuli visuels et auditifs, offrir des options, réduire la taille des espaces et le nombre d’occupants du lieu de vie, etc.).
- Les ressources communautaires offertes aux personnes atteintes et à leurs proches sont suffisamment variées pour répondre aux besoins complexes que vivent ces personnes. Parmi ces ressources, mentionnons, entre autres, la Société Alzheimer du Canada et ses divisions provinciales et régionales, les groupes de soutien pour les proches aidants et les programmes dans les hôpitaux de jour permettant aux proches aidants et aux familles d’avoir un répit, tandis que les personnes atteintes de la maladie peuvent y faire diverses activités stimulant leurs sens et leurs capacités cognitives.
L’approche interdisciplinaire prônée par les équipes interprofessionnelles fait en sorte que les personnes peuvent conserver leur autonomie sur une plus grande période de temps et offre un soutien aux familles pour les aider à composer avec la maladie de leur proche. Travailleurs sociaux, ergothérapeutes, médecins, infirmières, psychologues et orthophonistes s’allient souvent pour soutenir les personnes et leur entourage.
Pronostic
Même si incompréhensions sont encore nombreuses dans le domaine des atteintes neurocognitives, le déclin associé à ces atteintes, particulièrement dans les capacités cognitives des personnes, est clair et inévitable. Lorsque la personne atteint un stade avancé de la maladie, elle perd souvent la capacité de prendre soin d’elle-même et il en résulte que les proches doivent généralement offrir une somme importante de soins. Éventuellement, l’hébergement en centre de soins de longue durée sera inévitable. Le décès de la personne survient dans beaucoup de cas suite à une infection qui n’a pas été détectée ou un syndrome de déconditionnement provoqué par la perte des capacités fonctionnelles et de mobilisation. Dans la mesure où l’avancement en âge fait en sorte qu’il est plus difficile de diagnostiquer une infection en raison de l’absence de fièvre et de réaction leucocytaire, les infections ne sont pas rares dans cette population. Cela s’avère d’ailleurs d’autant plus chez les personnes ayant une atteinte neurocognitive, ne pouvant souvent pas faire état des symptômes ressentis ou de l’inconfort vécu. La mort peut aussi survenir suite à l’incapacité de la personne de s’hydrater ou de s’alimenter. L’espérance de vie est souvent ainsi réduite pour les personnes vivant une atteinte neurocognitive, plusieurs mentionnent sept ans en moyenne après le diagnostic et six mois quand la marche n’est plus possible, mais il n’est pas rare de voir des personnes ayant ce type d’atteinte vivre bien au-delà de l’espérance de vie habituelle. Dans tous les cas, le pronostic est donc sombre. Cependant, si la qualité de vie peut être maintenue pendant le déclin des fonctions, la personne atteinte peut vivre ces années avec un sentiment de bonheur.
Références
- The Merck Manual (2014). Alzheimer Disease. Récupérée au :
http://www.merckmanuals.com/professional/neurologic_disorders/delirium_and_dementia/alzheimer_disease.html - The Merck Manual (2014). Dementia. Récupérée au :
http://www.merckmanuals.com/professional/neurologic_disorders/delirium_and_dementia/dementia.html - The Merck Manual (2014). Récupérée au :
http://www.merckmanuals.com/professional/neurologic_disorders/delirium_and_dementia/vascular_dementia.html - The Merck Manual (2014). Lewy body dementia and Parkinson disease dementia. Récupérée au :
http://www.merckmanuals.com/professional/neurologic_disorders/delirium_and_dementia/lewy_body_dementia_and_parkinson_disease_dementia.html - The Merck Manual (2014). Frontotemporal dementia. Récupérée au :
http://www.merckmanuals.com/professional/neurologic_disorders/delirium_and_dementia/frontotemporal_dementia.html - Alzheimer’s Disease. Dans ATCHINSON, Ben J. et Diane K. DIRETTE, Conditions in Occupational Therapy : Effect on Occupational Performance (pp.102-117). Baltimore : Lippincott Wiliams & Wilkins.
- Vascular Dementia. Dans ATCHINSON, Ben J. et Diane K. DIRETTE, Conditions in Occupational Therapy : Effect on Occupational Performance (pp.117-118). Baltimore : Lippincott Wiliams & Wilkins.
- Frontotemporal Dementia. Dans ATCHINSON, Ben J. et Diane K. DIRETTE, Conditions in Occupational Therapy : Effect on Occupational Performance (pp.118-119). Baltimore : Lippincott Wiliams & Wilkins.
- Dementia with Lewy Bodies. Dans ATCHINSON, Ben J. et Diane K. DIRETTE, Conditions in Occupational Therapy : Effect on Occupational Performance (pp.119-120). Baltimore : Lippincott Wiliams & Wilkins.
- Alzheimer’s Disease. Dans DAMJANOV, Ivan. (2012). Pathology for the Health Professions. (pp.466-467). 4e édition. Misouri : Elsevier Saunders.
- Alzheimer’s Disease. Dans VANMETER, Karin C. and Robert J. HUBERT. (2014). Gould’s Pathophysiology for the Health Professions (pp.376-377). 5e édition, Misouri : Elsevier Saunders
- Other forms of Dementia. Dans VANMETER, Karin C. and Robert J. HUBERT. (2014). Gould’s Pathophysiology for the Health Professions (pp.377-378). 5e edition, Misouri : Elsevier Saunders.
- Alzheimer Society. (2010). Rising Tide L The impact of dementia on Canadian Society. Alzheimer Society of Canada. Consulté le 16 juillet 2014 au : https://alzheimer.ca/sites/default/files/files/national
/advocacy/asc_rising_tide_full_report_e.pdf
Outils technologiques de rédaction :
- TERMIUM plus : http://www.btb.termiumplus.gc.ca/tpv2alpha/alpha-fra.html?lang=fra
- Larousse en ligne : http://www.larousse.fr/dictionnaires/francais
- Linguee: http://www.linguee.fr/francais-anglais